¿Puede el ejercicio frenar la progresión de la esclerosis múltiple? Esclerosis múltiple, o esclerosis múltiple, Es una enfermedad crónica, neurológica, caracterizada por el daño a las vainas de mielina de las células nerviosas en el sistema nervioso central o SNC. Los síntomas comunes de la esclerosis múltiple incluyen dolor, fatiga, pérdida de la visión y alteración de la coordinación. El ejercicio con frecuencia se recomienda como una forma de tratamiento para varios tipos de lesiones y / o afecciones, incluida la EM. Si bien se ha determinado que el ejercicio ayuda a mejorar el manejo de los síntomas de la esclerosis múltiple y disminuye la progresión de la enfermedad, aún se requieren pruebas adicionales. El propósito del siguiente artículo es demostrar cómo el ejercicio puede afectar la progresión de la enfermedad de la esclerosis múltiple y mejorar la calidad de vida de los pacientes.
Resumen
Se ha sugerido que el ejercicio (o la actividad física) podría tener el potencial de tener un impacto en la patología de la esclerosis múltiple (EM) y, por lo tanto, retardar el proceso de la enfermedad en pacientes con EM. El objetivo de esta revisión de la literatura fue identificar la literatura que vincula el ejercicio físico (o actividad) y la progresión de la enfermedad de la EM. Se realizó una búsqueda bibliográfica sistemática en las siguientes bases de datos: PubMed, SweMed +, Embase, Biblioteca Cochrane, PEDro, SPORTDiscus e ISI Web of Science. Se han aplicado diferentes enfoques metodológicos para el problema, incluidos (1) estudios de ejercicios longitudinales que evalúan los efectos en las medidas de resultados clínicos, (2) estudios transversales que evalúan la relación entre el estado físico y los hallazgos de IRM, (3) estudios transversales y longitudinales evaluando la relación entre el ejercicio / actividad física y la tasa de discapacidad / recaída y, finalmente, los estudios de ejercicio longitudinal (4) que aplican el modelo animal de EM con encefalomielitis autoinmune experimental (EAE). Los datos de los estudios de intervención que evalúan la progresión de la enfermedad mediante medidas clínicas (1) no apoyan el efecto modificador de la enfermedad del ejercicio; sin embargo, los datos de IRM (2), los datos informados por el paciente (3) y los datos del modelo EAE (4) indican un posible efecto del ejercicio que modifica la enfermedad, pero la fuerza de la evidencia limita las conclusiones definitivas. Se concluyó que algunas pruebas apoyan la posibilidad de un potencial modificador de la enfermedad del ejercicio (o actividad física) en pacientes con EM, pero se necesitan estudios futuros que utilicen mejores metodologías para confirmar esto.
Palabras clave: Actividad de la enfermedad, terapia de ejercicios, actividad física, entrenamiento.
Introducción
La esclerosis múltiple (EM) es una enfermedad clínica y patológicamente compleja y heterogénea de etiología desconocida [Kantarci, 2008]. En los países europeos 28 con una población total de 466 millones de personas, se estima que las personas con 380,000 se ven afectadas por la EM [Sobocki et al. 2007]. El trastorno es progresivo, pero más del 80% de todos los pacientes con EM tienen la enfermedad durante más de 35 años [Koch-Henriksen et al. 1998], el número de años de vida perdidos por la enfermedad
Para obtener más información sobre este importante tema, por lo tanto, realizamos una búsqueda sistemática de la literatura con el objetivo de identificar estudios que relacionen el ejercicio (o la actividad física) con la progresión de la enfermedad en pacientes con EM o en el modelo animal de EM con encefalomielitis autoinmune experimental (EAE). Un propósito secundario de la revisión fue discutir los posibles mecanismos que explican este enlace si existe y discutir las futuras instrucciones de estudio dentro de este campo.
Métodos
La bibliografía incluida se identificó mediante una búsqueda bibliográfica exhaustiva (PubMed, SweMed+, Embase, Cochrane Library, PEDro, SPORTDiscus e ISI Web of Science) que se realizó para identificar artículos relevantes sobre la EM y el ejercicio hasta el 4 de septiembre de 2011. La búsqueda se realizó utilizando los encabezamientos de materia 'ejercicio', 'terapia de ejercicio', 'educación y entrenamiento físicos', 'aptitud física', 'actividad motora' o ' entrenamiento' en combinación con 'esclerosis múltiple' o 'encefalomielitis autoinmune experimental'. No se introdujeron limitaciones con respecto al año de publicación y la edad de los sujetos. De ser posible, se excluyeron resúmenes, comentarios y capítulos de libros al realizar la búsqueda en las diferentes bases de datos. Esta búsqueda arrojó 547 publicaciones.
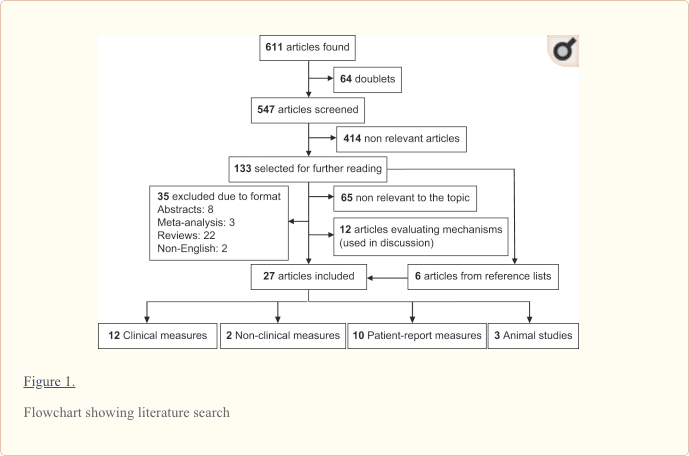
Según Goldman y sus colegas, las mediciones que se piensa que reflejan la progresión (o actividad) de la enfermedad en la EM pueden evaluarse con medidas de resultado objetivas o subjetivas [Goldman et al. 2010]. Las medidas objetivas incluyen (1) medidas de resultados clínicos tales como la Escala de estado de discapacidad expandida (EDSS) y el Compuesto funcional de esclerosis múltiple (MSFC) y (2) medidas no clínicas, como la RM. Las medidas subjetivas incluyen (3) medidas informadas por el paciente que se piensa que reflejan la progresión de la enfermedad o la discapacidad, como el Inventario de discapacidad y función de la vida tardía. Los estudios que aplicaron medidas informadas por los pacientes que incluían una medida de la actividad física también se incluyeron en esta categoría. Además, agregamos una categoría que contiene estudios que aplican (4) el modelo animal de EAE de MS como
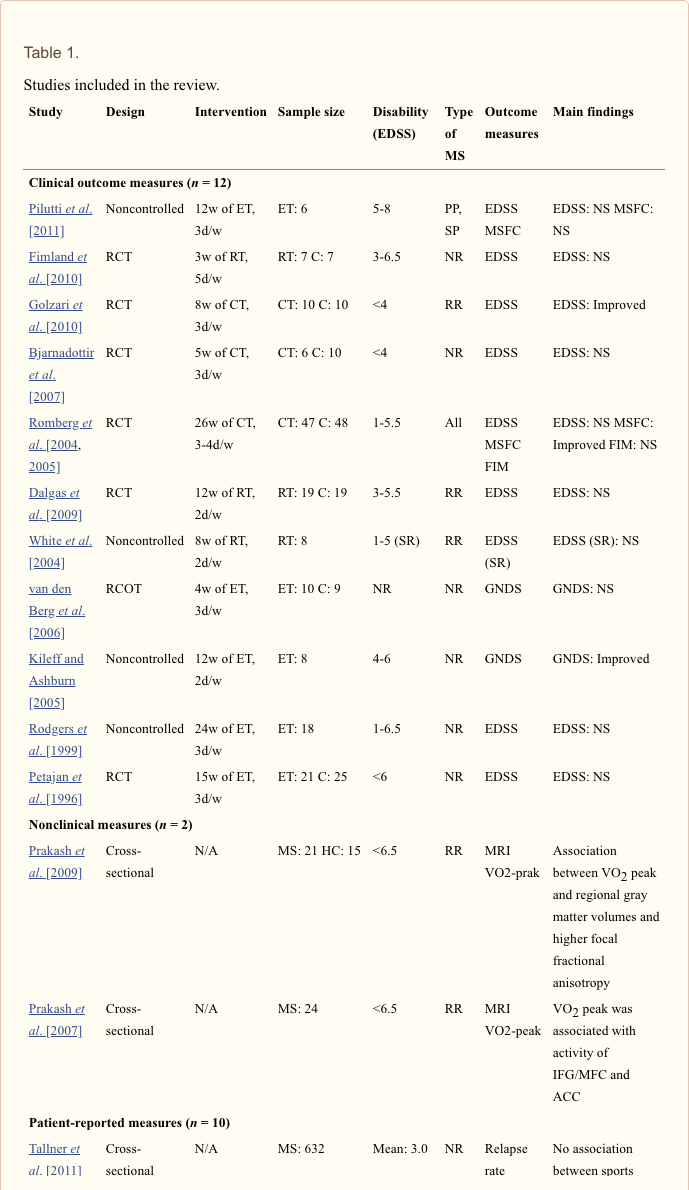
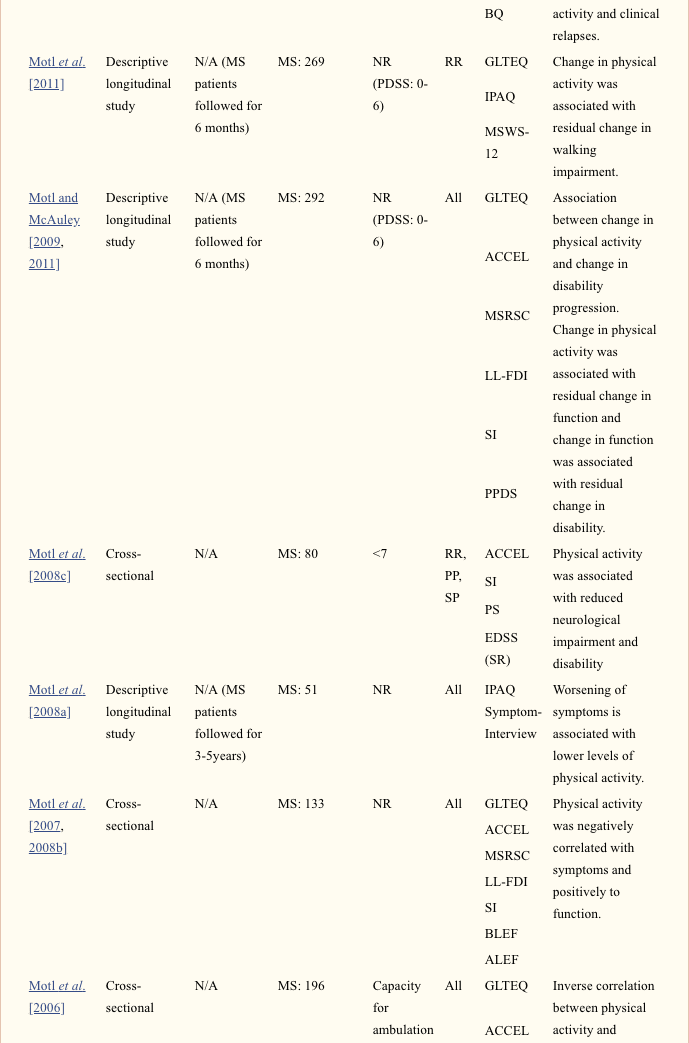
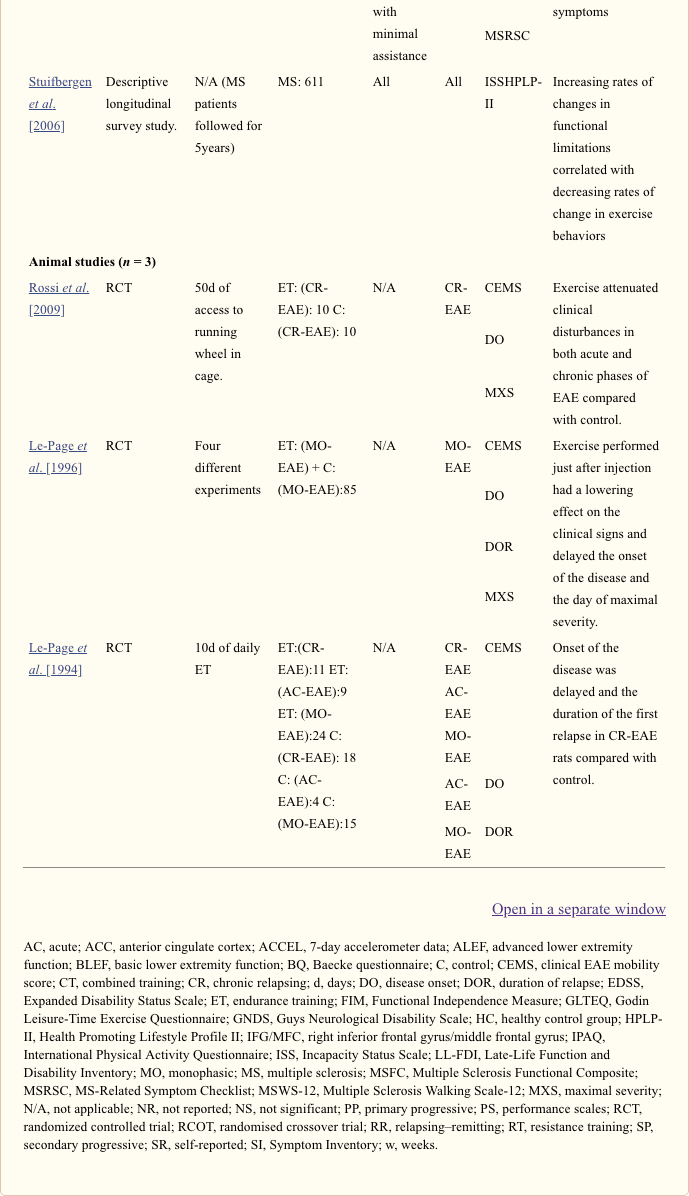
- progresión de la enfermedad evaluada con medidas de resultado clínico (n = 12);
- progresión de la enfermedad evaluada con medidas no clínicas (n = 2);
- progresión de la enfermedad evaluada con medidas informadas por el paciente (n = 10);
- Progresión de la enfermedad evaluada en estudios con animales (n = 3).
Resultados
Progresión de la enfermedad evaluada con medidas clínicas
Varios estudios que evaluaron intervenciones de ejercicios estructurados que duraron desde 3 hasta semanas 26 incluyeron escalas clínicas que reflejaban la progresión de la enfermedad como una medida de resultado. Las escalas clínicas aplicadas incluyen la EDSS [Bjarnadottir et al. 2007;
En resumen, los estudios de intervención de ejercicios estructurados de diferentes modalidades de ejercicio que duran de 3 a 26 semanas generalmente no han encontrado efectos en las puntuaciones de EDSS. Algunos estudios de ejercicio han mostrado efectos positivos al aplicar otras escalas clínicas (MSFC y GNDS).
Progresión de la enfermedad evaluada con medidas no clínicas
Dos estudios realizados por Prakash y sus colegas han evaluado los efectos de la aptitud cardiorrespiratoria en la función y estructura del cerebro mediante la aplicación de MRI (funcional) [Prakash et al. 2007, 2009]. Un estudio [Prakash et al. 2007] investigó el impacto de la aptitud cardiorrespiratoria en el funcionamiento cerebrovascular de los pacientes con EM. Veinticuatro mujeres participantes con
En otro estudio realizado por Prakash y colegas, se estudió la relación entre la capacidad cardiorrespiratoria (VO2 max) y las medidas de atrofia de la materia gris e integridad de la materia blanca (ambas relacionadas con el proceso de la enfermedad) [Prakash et al. 2009]. Se aplicó un enfoque basado en vóxels para el análisis de la materia gris y la materia blanca en el cerebro de un sistema de resonancia magnética 3-T. Más específicamente, se examinó si los niveles más altos de aptitud física en pacientes con EMN 21 se asociaron con el volumen de materia gris preservada y la integridad de la materia blanca. Se informó una asociación positiva entre la aptitud cardiorrespiratoria y los volúmenes regionales de materia gris y los valores más altos de anisotropía fraccional focal. Tanto el volumen de materia gris conservada como la integridad del tracto de materia blanca se asociaron con un mejor rendimiento en las medidas de velocidad de procesamiento. Al reconocer la naturaleza transversal de los datos, los autores sugirieron que la condición física ejerce una influencia profiláctica en el deterioro estructural observado en una etapa temprana, preservando la integridad neuronal en la EM, lo que reduce la discapacidad a largo plazo.
En resumen, (f) los estudios de resonancia magnética que sugieren un efecto protector de la aptitud cardiorrespiratoria sobre la función y estructura del cerebro en pacientes con EM han comenzado a emerger. Sin embargo, la naturaleza transversal de los pocos estudios existentes limita las conclusiones con respecto a la existencia de una relación causal.
Progresión de la enfermedad evaluada con medidas informadas por el paciente
Varios estudios han abordado la relación entre el ejercicio o la actividad física y la progresión de la enfermedad en estudios de cuestionario a gran escala que aplican medidas informadas por los pacientes.
En un gran estudio de encuesta longitudinal descriptivo, Stuifbergen y sus colegas examinaron las correlaciones entre el cambio en las limitaciones funcionales, los comportamientos de ejercicio y la calidad de vida [Stuifbergen et al. 2006]. Más de 600 pacientes con EM completaron una serie de cuestionarios cada año durante un período de 5 años. Las medidas longitudinales autoinformadas se analizaron mediante la aplicación de modelos de curvas latentes. La Escala de estado de incapacidad proporcionó una medida de las limitaciones funcionales debidas a la EM, mientras que el Perfil de estilo de vida promotor de la salud II proporcionó una medida del comportamiento de ejercicio. En el primer punto de prueba (prueba de referencia), los datos transversales mostraron una correlación negativa significativa (r = ≤ 0.34) entre las limitaciones funcionales y las conductas de ejercicio, lo que sugiere que al comienzo del estudio los niveles más altos de limitaciones funcionales se asociaron con niveles más bajos de ejercicio Los datos longitudinales del estudio mostraron que las tasas crecientes de cambios en las limitaciones funcionales se correlacionaron con tasas decrecientes de cambio en los comportamientos de ejercicio (r = ≤ 0.25). En otras palabras, estos hallazgos sugieren que los aumentos en los comportamientos de ejercicio se corresponden con menores tasas de cambio en las limitaciones funcionales. No se encontró correlación entre el grado inicial de limitación y la tasa continua de ejercicio, lo que llevó a los autores a sugerir que las personas con EM con diversos niveles de limitaciones podrían ralentizar la trayectoria de aumento de las limitaciones a largo plazo con una participación constante en el ejercicio.
Una serie de estudios de Motl y colegas han abordado la relación entre la actividad física, los síntomas, las limitaciones funcionales y la discapacidad en pacientes con EM. En un estudio transversal [Motl et al. 2006] en 196 pacientes con EM, se recopiló el número de síntomas dentro de los 30 días (Lista de verificación de síntomas relacionados con la EM) y la actividad física (Cuestionario de ejercicio de tiempo libre de Godin y datos del acelerómetro de 7 días). Después de modelar los datos, se encontró una relación directa entre los síntomas y la actividad física (r = 0.24), lo que indica que una mayor cantidad de síntomas resultó en una menor cantidad de actividad física. Sin embargo, los autores notaron que el diseño transversal excluye las inferencias sobre la dirección de la causalidad, y la actividad física podría afectar los síntomas del mismo modo que los síntomas afectan la participación en la actividad física. Cuando se modeló de esta manera, se encontró una correlación inversa moderada entre la actividad física y los síntomas (r = ≤ 0.42), lo que indica menos síntomas cuando el nivel de actividad física es alto. Esto llevó a los autores a sugerir la existencia de una relación bidireccional entre la actividad física y los síntomas.
En un siguiente estudio de cuestionario, Motl y sus colegas examinaron la actividad física (Cuestionario de ejercicio de tiempo libre de Godin y datos del acelerómetro de 7 días) y los síntomas (Inventario de síntomas y Lista de verificación de síntomas relacionados con la EM) como correlatos de limitaciones funcionales y discapacidad (Función y discapacidad en la vejez). Inventory) en 133 pacientes con EM [Motl et al. 2007, 2008b]. Se probó un modelo basado en el modelo de discapacidad propuesto por Nagi (1976) como modelo primario y mostró que la actividad física y los síntomas estaban negativamente correlacionados (r = ≤ 0.59) y aquellos que eran más activos físicamente tenían una mejor función (r = 0.4). Además, aquellos con una mejor función tenían menos discapacidad (r = 0.63), lo que llevó a los autores a concluir que los hallazgos indican que la actividad física se asocia con una discapacidad reducida (a través de una asociación con la función) de acuerdo con el modelo de discapacidad de Nagi (Nagi 1976). ), pero nuevamente el diseño transversal limitó conclusiones definitivas sobre la dirección de las relaciones.
Motl y sus colegas publicaron un estudio longitudinal (informe de caso) que examinaba la relación entre el empeoramiento de los síntomas y el nivel de actividad física durante un período de 3 a 5-año [Motl et al. 2008a]. El estudio mostró que el empeoramiento de los síntomas (entrevista) se asoció significativamente con niveles más bajos de actividad física autoinformada (Cuestionario Internacional de Actividad Física [IPAQ]) en un grupo de sujetos 51 con EM. El estudio apoya los síntomas como una posible explicación de la tasa de inactividad física entre los pacientes con EM, pero aún no se pudo establecer la dirección de la relación de causa y efecto. Basados en los resultados, los autores sugieren que el manejo de los síntomas podría ser importante para la promoción de la actividad física, pero también que los síntomas pueden ser tanto un antecedente como una consecuencia de la actividad física.
Después de eso, Motl y sus colegas publicaron un estudio transversal que examinó la correlación entre la actividad física y el deterioro y la discapacidad neurológicos en un grupo de 80 pacientes con EM [Motl et al. 2008c]. Se midió la actividad física (día del acelerómetro de 7 días), el deterioro y la discapacidad (Inventario de Síntomas y EDSS autoinformado) y se encontraron correlaciones significativas entre la actividad física y tanto el EDSS (r = 0.60) como el Inventario de Síntomas (r = 0.56). XNUMX). Los autores concluyeron que la actividad física se asoció con una reducción del deterioro neurológico y la discapacidad, pero también afirmaron que no se pudo establecer una relación causal debido a la naturaleza transversal del estudio.
Luego, Motl y McAuley publicaron un estudio de cuestionario longitudinal a gran escala que examinaba los cambios en la actividad física (Cuestionario de ejercicio de tiempo libre de Godin y datos del acelerómetro de 7 días) y síntomas (Inventario de síntomas y Lista de verificación de síntomas relacionados con la EM) como correlatos de cambios en funcional limitaciones y discapacidad (Late-Life Function and Disability Inventory) [Motl y McAuley, 2009]. Un total de 292 pacientes con EM fueron seguidos durante 6 meses. Nuevamente, se probó un modelo basado en el modelo de discapacidad propuesto por Nagi (1976) como modelo primario y esto mostró que el cambio en la actividad física se asoció con un cambio residual en la función (r = 0.22) y el cambio en la función se asoció con un cambio residual en la función. discapacidad (r = 0.20). Esto llevó a los autores a concluir que los hallazgos indican que el cambio en la actividad física está asociado con un cambio en la discapacidad (a través de una asociación con la función) consistente con el modelo de discapacidad de Nagi, pero se pueden aplicar otros modelos durante el análisis y una interpretación causal. por lo tanto, todavía no podía ser adoptado.
En un estudio longitudinal de 6 meses, Motl y sus colegas probaron la hipótesis de que un cambio en la actividad física (Cuestionario de ejercicio de tiempo libre de Godin y Cuestionario internacional de actividad física) estaría inversamente asociado con un cambio en el deterioro de la marcha (Escala de marcha de esclerosis múltiple-12 ) en pacientes con EM recurrente-remitente [Motl et al. 2011a]. Los datos de 263 pacientes con EM se analizaron mediante análisis de panel lineal y modelado de covarianza. Los hallazgos mostraron que un cambio en la unidad de desviación estándar de 1 en la actividad física se asoció con un cambio residual en la unidad de desviación estándar de 0.16 en el deterioro de la marcha. Estos hallazgos, por lo tanto, respaldan la actividad física como un enfoque importante, cuando se trata de evitar las dificultades para caminar.
Finalmente, Motl y McAuley publicaron un artículo sobre datos longitudinales (6 meses) de 292 pacientes con EM que evaluaron la relación entre un cambio en la actividad física (datos del acelerómetro de 7 días) y un cambio en la progresión de la discapacidad (Patient Determined Disease Steps Scale) [Motl y MacAuley, 2011]. El análisis de panel mostró que un cambio en la actividad física se asoció con un cambio en la progresión de la discapacidad (coeficiente de trayectoria: -0.09). Esto llevó a los autores a concluir que una reducción en la actividad física es un correlato conductual (pero no necesariamente una causa) de la progresión de la discapacidad a corto plazo en personas con EM.
Recientemente, Tallner y sus colegas evaluaron la relación entre la actividad deportiva (Cuestionario de Baecke, índice deportivo) y las recaídas de la EM durante los últimos 2 años (según autoinformes) en 632 pacientes alemanes con EM [Tallner et al. 2011]. Los pacientes se dividieron en cuatro grupos según su índice deportivo. El estudio no mostró diferencias generales entre los cuatro grupos con respecto al número de recaídas en los últimos 2 años. Sin embargo, el grupo más activo tuvo la media y la desviación estándar más bajas de todos los grupos. En consecuencia, estos datos sugieren que el ejercicio no influye negativamente en la tasa de recaídas y los datos indican además que el ejercicio en realidad reduce la tasa de recaídas.
En resumen, las medidas informadas por los pacientes de la asociación entre el ejercicio o la actividad física y la progresión de la enfermedad (expresada como síntomas, limitaciones funcionales o discapacidad) o la actividad (tasa de recaída) proporcionan evidencia de una asociación con más actividad física que brinda protección. Sin embargo, debido a la naturaleza de los estudios, no se ha establecido la causalidad de esta asociación.
Progresión de la enfermedad evaluada en estudios con animales
Algunas dificultades metodológicas obvias.
En un estudio preliminar realizado por Le-Page y colegas, se siguió a cuatro grupos de ratas EAE desde el día 1 hasta el día 10 después de la inyección con un agente que inducía la EAE [Le-Page et al. 1994]. La inyección resultó en tres cursos diferentes de enfermedad en las ratas, a saber, aguda (las ratas desarrollaron rápidamente signos clínicos graves y murieron sin signos de recuperación), monofásica (las ratas desarrollaron solo un episodio de enfermedad seguido de una recuperación completa) y crónica recidivante (CR-EAE , más de un episodio de enfermedad seguido de remisión). El curso de la enfermedad CR-EAE se caracteriza por el desarrollo de un ataque paralítico agudo inicial 10 a 20 días después de la inmunización con neuroantígenos y el desarrollo de recaídas espontáneas posteriormente. Un grupo de ratas macho y hembra ejercitaron y un grupo macho y hembra sirvieron como control. El ejercicio consistió en correr en una cinta rodante desde el día 1 hasta el día 10 después de la inyección. El protocolo se ajustó progresivamente aumentando la duración de 60 min a 120 min y la velocidad de carrera aumentando de 15 a 30 m/min. El estudio mostró que en las ratas CR-EAE ejercitadas de ambos sexos, la aparición de la enfermedad se retrasó significativamente en comparación con la aparición en las ratas CR-EAE de control. Además, la duración de la primera recaída se redujo significativamente en las ratas CR-EAE ejercitadas en comparación con las ratas de control, mientras que no se observó ningún efecto sobre la gravedad máxima de la enfermedad. No se observaron efectos del ejercicio en las ratas con EAE aguda y monofásica. Los autores concluyeron que el ejercicio de resistencia durante la fase de inducción de la EAE disminuyó levemente un tipo de EAE (CR-EAE) pero también que el ejercicio no exacerbó la enfermedad.
En un estudio complementario, Le-Page y sus colegas realizaron otros cuatro experimentos en el modelo EAE monofásico [Le-Page et al. 1996]. Los experimentos 1 y 2 mostraron que 2 días consecutivos de ejercicio intenso (250-300 min/día) realizados justo después de la inyección tuvieron un efecto de reducción en el curso de los signos clínicos de la enfermedad en comparación con las ratas de control. Además, el inicio de la enfermedad y el día de máxima gravedad se retrasaron en las ratas que hacían ejercicio, mientras que no se observaron cambios en la duración de la enfermedad. Cuando los 2 días consecutivos de ejercicio se realizaron antes de la inyección, no se observaron efectos. En los experimentos 3 y 4 se probó cómo 5 días de ejercicio más moderado a velocidad constante (15-25 m/min durante 2 horas) o variable (3 min a 2 m/min y luego 2 min a 35 m/min). durante un total de 1 hora) afectó el curso de la enfermedad y los parámetros clínicos. No se observaron efectos sobre el curso de la enfermedad y sobre los parámetros clínicos. Los autores concluyeron que el ejercicio intenso frente al ejercicio más moderado influyó ligeramente en la fase efectora de la EAE monofásica y confirmaron que el ejercicio físico realizado antes del inicio de la EAE no exacerbó los signos clínicos.
Más recientemente, Rossi y sus colegas exploraron más a fondo los efectos de la actividad física sobre la progresión de la enfermedad en el modelo de ratones CR-EAE [Rossi et al. 2009]. En este estudio, un grupo de ratones tenía su jaula equipada con una rueda para correr el día de la inmunización, mientras que el grupo de control no tenía rueda para correr. No se controló la cantidad de actividad física y, por lo tanto, fue la cantidad de actividad física voluntaria en la rueda de carrera lo que constituyó la intervención. En otro experimento, se compararon ratones EAE en jaulas estándar con ratones EAE en jaulas equipadas con una rueda bloqueada. Esto se hizo para diseccionar el papel de la actividad física del enriquecimiento sensorial causado por la propia rueda, y demostró que no influye en el curso clínico de la enfermedad. Durante la fase inicial (13 días después de la inyección) de la enfermedad, los ratones que hacían ejercicio corrieron espontáneamente un promedio de 760 vueltas/día en la rueda de carrera, que se redujo a 18 vueltas/día cuando el deterioro motor alcanzó su punto máximo (20-25 días después de la inyección). El estudio mostró que la gravedad de los trastornos clínicos inducidos por EAE se atenuó en las fases aguda y crónica de EAE en los ratones físicamente activos, que exhibieron déficits neurológicos menos graves en comparación con los animales EAE de control durante un período de tiempo de 50 días después de la inducción de EAE. . Además, se demostró que tanto los defectos sinápticos como dendríticos provocados por la EAE se atenúan con la actividad física.
En resumen, el ejercicio aeróbico (o actividad física voluntaria) tiene el potencial de influir en el curso clínico de la enfermedad en el modelo animal de EM de EAE.

Participar en actividades físicas y hacer ejercicio puede ser beneficioso para cualquier persona, especialmente para las personas con esclerosis múltiple o EM. El ejercicio puede ayudar a aliviar los síntomas de la esclerosis múltiple, sin embargo, los pacientes deben tener cuidado con la cantidad de actividad física que realizan. Varios estudios de investigación como el que se analiza en este artículo han determinado que las actividades físicas y los ejercicios pueden ayudar a mejorar los síntomas, así como a disminuir la velocidad. Baja la progresión de la esclerosis múltiple. Es esencial hablar con un profesional de la salud para discutir los detalles de cada programa de entrenamiento para poder aprovechar al máximo el Beneficios del ejercicio para la EM..
Dr. Alex Jimenez DC, CCST
Discusión
La evidencia reciente de los estudios que aplican medidas no clínicas y reportadas por el paciente, así como de los estudios que aplican el modelo animal de EM de la EAE, indica un posible efecto modificador de la enfermedad del ejercicio (o actividad física), pero la fuerza de la evidencia limita las conclusiones definitivas. Además, estos hallazgos no se confirman en los estudios de intervención que evalúan la progresión de la enfermedad mediante medidas de resultados clínicos. A pesar de las dificultades obvias asociadas, se necesitan futuros estudios de intervención con ejercicios a largo plazo en un gran grupo de pacientes con EM en este campo.
Enfermedad de pregresión
Algunos problemas metodológicos importantes surgen cuando se trata de medir la progresión de la enfermedad de la EM. La medida de resultado ideal para la EM cuantificaría la progresión irreversible de la enfermedad sostenida, pero en la EM esto ha resultado difícil. La expresión pleiotrópica de la EM hace que sea difícil medir todas las facetas de la enfermedad y puede ser necesario centrarse en síntomas específicos. Además, la gran heterogeneidad de los pacientes, la variabilidad de la población en el curso de la enfermedad y el ritmo de la progresión, los cambios subcutáneos en la resonancia magnética del impacto incierto en la progresión de la discapacidad retrasada, los déficits neurológicos multifacéticos con capacidades variadas para los pacientes individuales para compensar y las comorbilidades del paciente complican aún más las cosas [Goldman et al. 2010].
Resultado Clínico Mfacilidades
EDSS, MSFC y la tasa de recaída son las medidas de resultado clínicas estándar para los ensayos terapéuticos de EM y la medida de progresión de la enfermedad más utilizada es la EDSS [Goldman et al. 2010]. Nuestra revisión de la literatura muestra que los estudios de ejercicio (resistencia, resistencia y entrenamiento combinado) que aplican EDSS generalmente no informan ningún cambio después de una intervención de ejercicio. En los estudios médicos que aplican EDSS, se requieren típicamente muestras de gran tamaño e intervenciones que duran de 2 a 3 años para medir los cambios en las tasas de exacerbación entre el tratamiento y el placebo [Bates, 2011]. Esto se corresponde mal con los cortos períodos de intervención (3 a 26 semanas) y los pequeños tamaños de muestra aplicados en la mayoría de los estudios de ejercicios. Esto se debe a la baja capacidad de respuesta y sensibilidad general al cambio del EDSS, como se informó en una serie de estudios (para referencias, consulte Goldman et al. [2010]). Además, las EDSS han sido criticadas por su
Además de la capacidad de respuesta a baja escala, las intervenciones a corto plazo y los tamaños de muestra pequeños, se pueden plantear como hipótesis otras explicaciones de la falta general de efectos sobre las medidas de resultado clínico. A pesar de que no hay un patrón claro en los datos existentes, el tipo de ejercicio (por ejemplo, entrenamiento de resistencia versus entrenamiento de resistencia) puede influir en el efecto capturado por las escalas clínicas. Además, la mayoría de los estudios han evaluado a pacientes con EM con deterioro leve a moderado (EDSS <6). Quizás las escalas clínicas serían más sensibles al cambio en pacientes más gravemente deteriorados. Por último, los resultados pueden estar sesgados si, en general, son los pacientes en mejor forma física los que aceptan participar en estudios de ejercicio. Si es así, el nivel de condición física inicial puede estar por encima del promedio en estos pacientes, lo que reduce aún más la posibilidad de un cambio en las escalas clínicas con baja capacidad de respuesta.
Sólo unos pocos estudios [Bjarnadottir et al. 2007; Petajan et al. 1996; Romberg et al. 2004; White et al. 2004] presenta datos claros sobre la tasa de recaída, pero debido a los cortos períodos de intervención y los pequeños tamaños de muestra en la mayoría de los estudios, no se espera que los cambios en la tasa de recaída sean evidentes. Sin embargo, Romberg y sus colegas encontraron un total de recaídas de 11 (cinco en el grupo de entrenamiento combinado y seis en el grupo de control) durante un período de intervención de 6-mes [Romberg et al. 2004]. De manera similar, Petajan y sus colegas (grupo de entrenamiento de resistencia cuatro recaídas y grupo de control tres recaídas) [Petajan et al. 1996] y Bjarnadottir y colegas (grupo de entrenamiento combinado una recaída y grupo de control una recaída) [Bjarnadottir et al. 2007] informó tasas de recaída idénticas en los grupos de ejercicio y control. En el estudio de White y sus colegas, ningún participante experimentó recaídas durante la intervención de 8-week que evaluó el entrenamiento de resistencia [White et al. 2004]. Recientemente, Tallner y sus colegas recopilaron cuestionarios de autoinforme sobre las tasas de recaída y la actividad física de pacientes con EM para examinar la relación de los diferentes niveles de actividad deportiva y recaídas [Tallner et al. 2011]. Sobre la base de estos datos, los autores concluyeron que el ejercicio no tuvo una influencia significativa en la actividad de la enfermedad clínica. En conjunto, los pocos datos existentes no indican que ningún tipo de ejercicio aumente la tasa de recaída entre los pacientes con EM. Sin embargo, estos datos deben interpretarse con precaución debido al pequeño número de participantes (no estratificados según el tipo de enfermedad o la gravedad) y los cortos períodos de intervención en la mayoría de los estudios. En consecuencia, los futuros estudios a largo plazo con un gran número de participantes deben, por lo tanto, incluir la tasa de recaída como una medida de resultado.
No clínico mfacilidades
La aplicación de la RM ha revolucionado el diagnóstico y el tratamiento de los pacientes con EM [Bar-Zohar et al. 2008]. En lo que respecta a los ensayos clínicos, la RM ofrece varias ventajas sobre las medidas de resultado clínicas aceptadas para la EM, que incluyen una mayor sensibilidad a la actividad de la enfermedad y una mejor asociación con los hallazgos histopatológicos. Además, la RM proporciona medidas altamente reproducibles en escalas ordinales, y la evaluación de la RMN se puede realizar en el mayor grado de cegamiento [Bar-Zohar et al. 2008]. En consecuencia, una IRM de sustitución mide la progresión de la enfermedad, como la actividad de la lesión (lesiones mejoradas con gadolinio y lesiones hiperintensas de T2 nuevas o agrandadas) o la gravedad de la enfermedad (volumen de la lesión hiperintensa de T2 total, volumen de lesión hipointensa total de T1 y atrofia cerebral total) [Bermel et al. 2008] puede reducir los tamaños de muestra requeridos necesarios para evaluar considerablemente los efectos del tratamiento con ejercicios en la progresión de la enfermedad. Hasta ahora, solo dos estudios transversales han evaluado los efectos del ejercicio (expresado como el nivel actual de aptitud cardiorrespiratoria) en diferentes medidas de RM que limitan las conclusiones que se pueden extraer de este tipo de estudio. Sin embargo, los resultados prometedores alientan la inclusión de la RM como una medida de resultado, en futuros ensayos longitudinales que evalúan los efectos del ejercicio sobre la progresión de la enfermedad.
Reporte del paciente Mfacilidades
Las medidas informadas por el paciente de la asociación entre el ejercicio o la actividad física y la progresión de la enfermedad (expresadas como síntomas, limitaciones funcionales o discapacidad) proporcionan evidencia de una asociación con más actividad física que brinda protección. Sin embargo, la naturaleza de los estudios no permite conclusiones sobre la causalidad de esta asociación. En el grupo de estudios aplicados a pacientes reportados.
Una ventaja importante de la aplicación de medidas informadas por los pacientes es la oportunidad de recopilar datos de muestras de gran tamaño en estudios longitudinales. Además, parece importante recopilar datos sobre la perspectiva del paciente al evaluar los efectos del ejercicio sobre la progresión de la enfermedad. Los estudios futuros que incluyan medidas informadas por el paciente también deben incluir medidas de resultado clínicas y / o no clínicas, de ser posible.
Animal studis
Nuestra revisión mostró que el ejercicio aeróbico (o actividades) tiene el potencial de influir en el curso clínico de la enfermedad en el modelo animal de EM de EAE. La pregunta obvia es si los hallazgos del modelo animal de EM de EAE se pueden extrapolar a los humanos. Por el momento no se puede dar una respuesta clara a esta pregunta. Una revisión reciente resumió si los tratamientos actuales que modifican la enfermedad se justifican sobre la base de los resultados de los estudios de EAE. Aquí se llegó a la conclusión de que, aunque la EAE es ciertamente un espejo imperfecto de la EM, muchos hallazgos clínicos, inmunopatológicos e histológicos se replican de manera impresionante mediante modelos animales, lo que hace que la EAE sea inestimable para dilucidar los mecanismos inmunopatológicos básicos de la EM y proporciona un campo de pruebas para terapias novedosas [Farooqi et al. 2010]. En consecuencia, no se puede realizar una transferencia directa de hallazgos a sujetos humanos, pero aquí pueden comenzar las pruebas de hipótesis difíciles. Además, debe tenerse en cuenta que en EAE no puede controlar la intensidad relativa del ejercicio, ya que no se puede realizar una prueba de ejercicio máxima (como una prueba de VO2 max). Como un
Posible mmecanismos
Se han propuesto varios mecanismos como un posible vínculo entre el ejercicio y el estado de la enfermedad en la EM. Algunos de los candidatos más prometedores incluyen citoquinas y factores neurotróficos [White and Castellano, 2008a].
Citoquinas. Las citoquinas juegan un papel importante en la patogenia de la EM y son un objetivo importante para las intervenciones de tratamiento. En particular, la interleucina (IL)-6, el interferón (IFN)-γ y el factor de necrosis tumoral (TNF)-α tienen un papel destacado en el proceso de desmielinización y daño axonal que experimentan las personas con EM [Compston and Coles, 2008] .
Los cambios en las concentraciones de ciertas citoquinas, en particular IFN-α y TNF-α, se han asociado con cambios en el estado de la enfermedad en la EM y concentraciones elevadas de citoquinas proinflamatorias Th-1 (como TNF-α, IFN -γ, IL-2 e IL-12) pueden contribuir a la neurodegeneración y la discapacidad [Ozenci et al. 2002]. Esto ha llevado a la sugerencia de que el ejercicio puede contrarrestar los desequilibrios entre las citocinas Th1 proinflamatorias y las citocinas Th2 antiinflamatorias (como IL-4 e IL-10) al mejorar los mecanismos antiinflamatorios y, por lo tanto, potencialmente ser capaz de alterar la actividad de la enfermedad en pacientes con EM [White y Castellano, 2008b].
En la EM, tanto los efectos agudos como los crónicos de la resistencia [White et al. 2006], resistencia [Castellano et al. 2008; Heesen et al. 2003; Schulz et al. 2004] y entrenamiento combinado [Golzari et al. 2010] en varias citoquinas han sido evaluadas. Un estudio realizado por White y colegas informó que los niveles de reposo de IL-4, IL-10, proteína C reactiva (PCR) e IFN-γ se redujeron, mientras que los niveles de TNF-α, IL-2 e IL-6 permanecieron sin cambios después 8 semanas de entrenamiento de resistencia quincenal [White et al. 2006]. Estos resultados sugieren que el entrenamiento de resistencia progresivo puede tener un impacto en las concentraciones de citoquinas en reposo y, por lo tanto, podría tener un impacto en la función inmunológica general y el curso de la enfermedad en personas con EM. Sin embargo, el estudio no fue controlado y solo se incluyeron 10 participantes, lo que obviamente limita la solidez de la evidencia. Heesen y sus colegas evaluaron los efectos agudos de 8 semanas de entrenamiento de resistencia sobre IFN-γ, TNF-α e IL-10 y compararon esto con un grupo de control de EM en lista de espera y un grupo de sujetos sanos emparejados [Heesen et al. 2003]. Después de completar 30 minutos de entrenamiento de resistencia (ciclismo), se indujo un aumento en IFN-γ de manera similar en todos los grupos, mientras que se observaron tendencias hacia aumentos más pequeños en TNF-α e IL-10 en los dos grupos de pacientes con EM. Basándose en estos datos, los autores concluyeron que no se pudo demostrar ninguna desviación en la respuesta inmunitaria proinflamatoria al estrés físico en pacientes con EM. Estos hallazgos, por lo tanto, respaldan que una sola sesión de entrenamiento de resistencia puede influir en el perfil de citoquinas al menos durante un período de tiempo en pacientes con EM. En otra publicación del mismo estudio, Schulz y sus colegas no pudieron demostrar ninguna diferencia entre el nivel de reposo o la respuesta aguda de IL-6 después de 30 minutos de ejercicio de resistencia en el grupo de entrenamiento con EM (8 semanas de ciclismo) y el grupo de control con EM. [Schulz et al. 2004].
Un estudio realizado por Castellano y colegas evaluó los efectos de 8 semanas de entrenamiento de resistencia (ciclismo, 3 días a la semana) sobre IL-6, TNF-α e IFN-γ en 11 pacientes con EM y 11 controles sanos emparejados. En pacientes con EM, tanto el IFN-α como el TNF-α en reposo se elevaron después del entrenamiento de resistencia, mientras que no se observaron cambios en los controles sanos [Castellano et al. 2008]. Como en el estudio de Heesen y colegas [Heesen et al. 2003], Castellano y sus colegas también estudiaron los efectos agudos de un solo turno de entrenamiento de resistencia y, de manera similar, no encontraron diferencias en comparación con los controles sanos, pero en este estudio no se observaron aumentos en IFN-γ y TNF-α en ninguno de los los grupos contrastaron los hallazgos de Heesen y sus colegas.
En el estudio más reciente, Golzari y sus colegas realizaron un ensayo controlado aleatorio (ECA) que evaluó los efectos de 8 semanas de entrenamiento combinado de resistencia y resistencia en IFN-γ, IL-4 e IL-17 [Golzari et al. 2010]. El estudio mostró reducciones significativas en las concentraciones de reposo de IFN-γ e IL-17 en el grupo de ejercicio, mientras que no se observaron cambios en el grupo de control, pero no se realizaron comparaciones de grupo.
En resumen, no se puede observar un patrón claro en las respuestas de citoquinas informadas al ejercicio que probablemente reflejen grandes diferencias metodológicas entre los estudios (tipo de estudio, tipo de intervención de ejercicio, tiempo de las mediciones, estandarizaciones, etc.) y un bajo poder estadístico que es crítico Debido a la gran variación en este tipo de medidas. No obstante, se ha informado que una sola serie de ejercicio influye en varias citoquinas (proinflamatorias) en pacientes con EM y también se han informado cambios crónicos en la concentración en reposo de varias citoquinas después de un período de entrenamiento. Además, la respuesta parece ser comparable a la de los sujetos sanos. Las citoquinas, por lo tanto, pueden vincular el ejercicio y la progresión de la enfermedad en la EM, pero los ECA futuros a gran escala tienen que evaluar esto más a fondo.
Factores neurotróficos. Los factores neurotróficos son una familia de proteínas que se cree que desempeñan un papel en la prevención de la muerte neuronal y favorecen el proceso de recuperación, la regeneración neural y la remielinización durante toda la vida [Ebadi et al. 1997]. Algunos de los factores neurotróficos mejor caracterizados incluyen el factor neurotrófico derivado del cerebro (BDNF) y el factor de crecimiento nervioso (NGF) [White and Castellano, 2008b].
Gold y sus colegas evaluaron los efectos agudos de un solo ejercicio (ciclo 30 min en 60% VO2 máx.) En NGF y BDNF en pacientes con 25 MS y compararon esto con un grupo de controles sanos compatibles [Gold et al. 2003]. El estudio mostró que las concentraciones iniciales de NGF eran significativamente más altas en pacientes con EM en comparación con los controles. Treinta minutos después del ejercicio, se observó un aumento significativo en BDNF, mientras que se observó una tendencia hacia un aumento en el NGF. Sin embargo, los cambios no difirieron de los cambios observados en los sujetos sanos. Esto hizo que los autores concluyeran que se puede usar ejercicio moderado para inducir la producción de neutrofina en sujetos con EM que posiblemente medien los efectos beneficiosos del ejercicio físico. En un estudio del mismo grupo, Schulz y sus colegas evaluaron los efectos del ciclo bisemanal de las semanas 8 en BDNF y NGF en un ECA en pacientes con EM [Schulz et al. 2004]. El estudio no mostró efectos en la concentración en reposo y en la respuesta al ejercicio agudo después del período de intervención, y solo se encontró una tendencia hacia niveles más bajos de NGF en reposo. Castellano y White también evaluaron si las semanas de ciclo de 8 (tres veces a la semana) afectarían las concentraciones séricas de BDNF en pacientes con EM y en controles sanos [Castellano y White, 2008]. En contraste con los hallazgos de Gold y sus colegas, el BDNF en reposo fue más bajo al inicio del estudio en pacientes con EM en comparación con los controles, pero no se encontraron diferencias (una tendencia) entre los grupos después de las semanas de 8. En pacientes con EM, la concentración de BDNF en reposo se elevó significativamente entre las semanas 0 y 4 y luego tendió a disminuir entre las semanas 4 y 8, mientras que la concentración de BDNF en reposo se mantuvo sin cambios en las semanas de entrenamiento de 4 y 8 en controles. Además, se evaluó la respuesta a una única serie de ejercicio que muestra una reducción significativa en BDNF 2 y 3 horas después del ejercicio en ambos grupos, lo que contrasta con los hallazgos de Gold y colegas. Los autores concluyeron que sus hallazgos proporcionaron evidencia preliminar que demuestra que el ejercicio puede influir en la regulación de BDNF en humanos.
En resumen, los resultados contrastantes sobre los efectos del ejercicio sobre los factores neurotróficos existen en pacientes con EM, lo que hace que se justifiquen más estudios. Sin embargo, los hallazgos implican que el ejercicio puede influir en varios factores neurotróficos que se sabe están involucrados en los procesos neuroprotectores.
Conclusiones
No se puede establecer claramente si el ejercicio tiene un efecto modificador de la enfermedad o no en pacientes con EM, pero existen estudios que indican que sí existen. Por lo tanto, se necesitan futuros estudios de intervención a largo plazo en un gran grupo de pacientes con EM para abordar esta importante pregunta.
AGRADECIMIENTOS
Los autores desean agradecer a la bibliotecaria de investigación Edith Clausen por su contribución sustancial a la búsqueda exhaustiva de la literatura.
Notas a pie de página
Esta investigación no recibió ninguna subvención específica de ninguna agencia de financiamiento en los sectores público, comercial o sin fines de lucro.
UD ha recibido becas de viaje y / o honorarios de Biogen Idec, Merck Serono.
La esclerosis múltiple, o EM, es una enfermedad crónica identificada por síntomas de dolor, fatiga, pérdida de la visión y coordinación alterada causada por el daño a las vainas de mielina de las células nerviosas en el sistema nervioso central o SNC. Se ha demostrado que el ejercicio ayuda a mejorar el manejo de los síntomas de la esclerosis múltiple y disminuye la progresión de la enfermedad, aunque aún se requieren pruebas adicionales, el artículo anterior resume estas medidas de resultado. El propósito del artículo anterior demuestra cómo el ejercicio puede cambiar la progresión de la esclerosis múltiple y mejorar la salud y el bienestar general. El alcance de nuestra información se limita a los problemas quiroprácticos y de salud de la columna vertebral. Para discutir el tema, no dude en preguntar al Dr. Jiménez o comuníquese con nosotros al
Comisariada por el Dr. Alex Jiménez
Remitido desde: Ncbi.nlm.nih.gov/pmc/articles/PMC3302199/

Tema adicional de discusión: Dolor de espalda agudo
El dolor de espalda es una de las causas más frecuentes de discapacidad y días perdidos en el trabajo en todo el mundo. El dolor de espalda se atribuye a la segunda razón más común para las visitas al consultorio del médico, superada únicamente por las infecciones de las vías respiratorias superiores. Aproximadamente el 80 por ciento de la población experimentará dolor de espalda al menos una vez a lo largo de su vida. La columna vertebral es una estructura compleja formada por huesos, articulaciones, ligamentos y músculos, entre otros tejidos blandos. Lesiones y / o condiciones agravadas, tales como hernias discales, eventualmente puede conducir a síntomas de dolor de espalda. Las lesiones deportivas o las lesiones por accidentes automovilísticos suelen ser la causa más frecuente de dolor de espalda; sin embargo, a veces los movimientos más simples pueden tener resultados dolorosos. Afortunadamente, las opciones de tratamiento alternativo, como la atención quiropráctica, pueden ayudar a aliviar el dolor de espalda mediante el uso de ajustes espinales y manipulaciones manuales, mejorando finalmente el alivio del dolor.

EXTRA EXTRA | TEMA IMPORTANTE: Quiropráctico recomendado en El Paso, TX»¿
***
Publicar descargos de responsabilidad
Alcance de la práctica profesional *
La información aquí contenida en "Ejercicio y progresión de la enfermedad en la esclerosis múltiple" no pretende reemplazar una relación personal con un profesional de la salud calificado o un médico con licencia y no es un consejo médico. Lo alentamos a que tome decisiones de atención médica basadas en su investigación y asociación con un profesional de la salud calificado.
Información del blog y debates sobre el alcance
Nuestro alcance informativo se limita a la quiropráctica, musculoesquelética, medicina física, bienestar, contribuyendo etiológico alteraciones viscerosomáticas dentro de las presentaciones clínicas, la dinámica clínica del reflejo somatovisceral asociado, los complejos de subluxación, los problemas de salud delicados y/o los artículos, temas y debates de medicina funcional.
Brindamos y presentamos colaboración clínica con especialistas de diversas disciplinas. Cada especialista se rige por su ámbito de práctica profesional y su jurisdicción de licencia. Utilizamos protocolos funcionales de salud y bienestar para tratar y apoyar la atención de lesiones o trastornos del sistema musculoesquelético.
Nuestros videos, publicaciones, temas, asuntos e ideas cubren cuestiones clínicas, problemas y temas que se relacionan y respaldan directa o indirectamente nuestro ámbito de práctica clínica.*
Nuestra oficina ha intentado razonablemente proporcionar citas de apoyo y ha identificado el estudio o los estudios de investigación relevantes que respaldan nuestras publicaciones. Proporcionamos copias de los estudios de investigación de respaldo disponibles para las juntas reguladoras y el público a pedido.
Entendemos que cubrimos asuntos que requieren una explicación adicional de cómo puede ayudar en un plan de atención o protocolo de tratamiento en particular; por lo tanto, para discutir más a fondo el tema anterior, no dude en preguntar Dr. Alex Jiménez, DC, o póngase en contacto con nosotros en 915-850-0900.
Estamos aquí para ayudarlo a usted y a su familia.
Bendiciones
El Dr. Alex Jimenez corriente continua MSACP, enfermero*, CCCT, IFMCP*, CIFM*, ATN*
email: coach@elpasomedicinafuncional.com
Licenciado como Doctor en Quiropráctica (DC) en Texas & New Mexico*
Número de licencia de Texas DC TX5807, Nuevo México DC Número de licencia NM-DC2182
Licenciada como Enfermera Registrada (RN*) en Florida
Licencia de Florida N.° de licencia de RN RN9617241 (Control No. 3558029)
Estado compacto: Licencia multiestatal: Autorizado para ejercer en 40 Estados*
Matriculado actualmente: ICHS: MSN* FNP (Programa de enfermera practicante familiar)
Dr. Alex Jiménez DC, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Mi tarjeta de presentación digital






 De nuevo te doy la bienvenida.
De nuevo te doy la bienvenida.
Los comentarios están cerrados.