El Paso, TX. Quiropráctico El Dr. Alexander Jiménez analiza varias condiciones que pueden causar dolor crónico. Éstas incluyen:
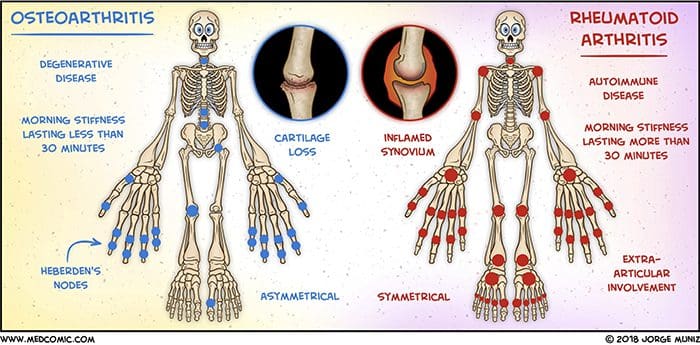
- Osteoartritis
- Dolor facetogénico
- El dolor neuropático
- dolores de cabeza
 Resumen
Resumen
Artritis el dolor es un fenómeno complejo que implica procesamiento neurofisiológico complejo en todos los niveles de la vía del dolor. Las opciones de tratamiento disponibles para aliviar dolor en las articulaciones son bastante limitadas y la mayoría de los pacientes con artritis informan un alivio del dolor moderado con los tratamientos actuales. Una mejor comprensión de los mecanismos neuronales responsables del dolor musculoesquelético y la identificación de nuevos objetivos ayudarán en el desarrollo de futuras terapias farmacológicas. Este artículo revisa algunas de las últimas investigaciones sobre los factores que contribuyen al dolor en las articulaciones y cubre áreas como los cannabinoides, los receptores de proteinasas activadas, los canales de sodio, las citoquinas y los canales transitorios de potenciales receptores. También se discute la hipótesis emergente de que la osteoartritis puede tener un componente neuropático.
Introducción
La organización mundial de la salud clasifica los trastornos musculoesqueléticos como la causa más frecuente de discapacidad en el mundo moderno, afectando a uno de cada tres adultos [1]. Aún más alarmante es que la prevalencia de estas enfermedades está aumentando, mientras que nuestro conocimiento de sus causas subyacentes es bastante rudimentario.
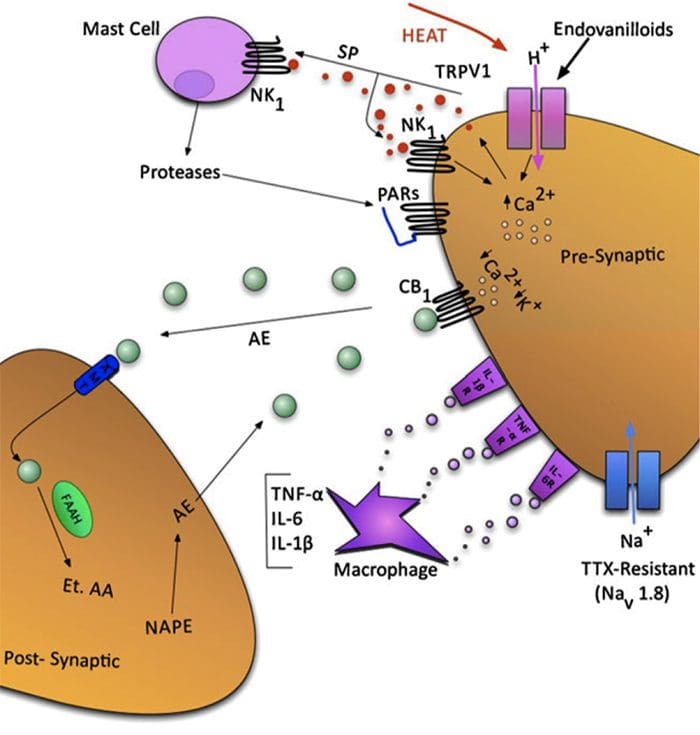
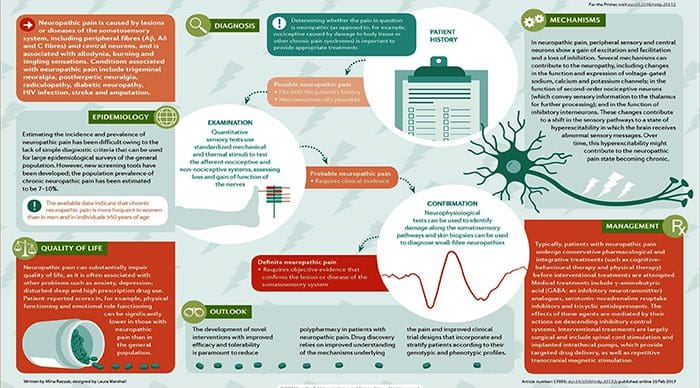
Fig. 1 Un esquema que ilustra algunos de los objetivos conocidos por modular el dolor articular. Los neuromoduladores pueden liberarse de las terminales nerviosas, así como de los mastocitos y los macrófagos para alterar la mecanosensibilidad aferente. Los endovaniloides, el ácido y el calor nocivo pueden activar los canales iónicos de potencial receptor transitorio vanilloide tipo 1 (TRPV1) que conducen a la liberación de sustancia algogénica P (SP) que posteriormente se une a los receptores de toneuroquinina-1 (NK1). Las proteasas pueden escindir y estimular los receptores activados por proteasa (PAR). Hasta ahora, se ha demostrado que PAR2 y PAR4 sensibilizan los aferentes primarios de las articulaciones. El endocannabinoide anandamida (AE) se produce bajo demanda y se sintetiza a partir de N-araquidonilfosfatidiletanolamina (NAPE) bajo la acción enzimática de fosfolipasas. Luego, una parte de AE se une a los receptores de cannabinoides-1 (CB1), lo que lleva a la desensibilización neuronal. El AE no unido es absorbido rápidamente por un transportador de membrana de anandamida (AMT) antes de ser descompuesto por una amida hidrolasa de ácido graso (FAAH) en etanolamina (Et) y ácido araquidónico (AA). El factor de necrosis tumoral de citoquinas-α (TNF-α), la interleucina-6 (IL-6) y la interleucina 1-beta (IL-1β) pueden unirse a sus respectivos receptores para mejorar la transmisión del dolor. Finalmente, existen canales de sodio resistentes a la tetrodotoxina (TTX) (Nav1.8) involucrados en la sensibilización neuronal.
Los pacientes anhelan por su dolor crónico desaparecer; sin embargo, los analgésicos recetados actualmente son en gran medida ineficaces y van acompañados de una amplia gama de efectos secundarios no deseados. Como tal, millones de personas en todo el mundo sufren los efectos debilitantes del dolor articular, para los cuales no existe un tratamiento satisfactorio [2].
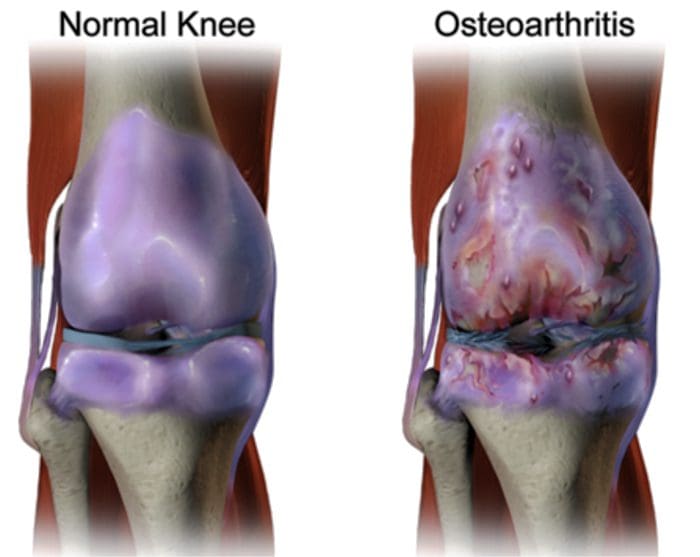
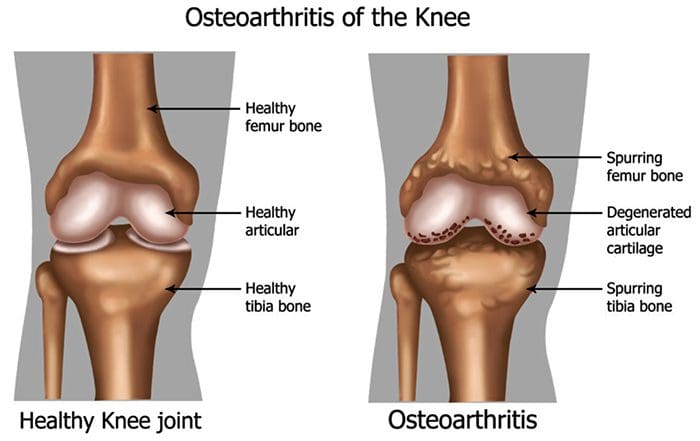
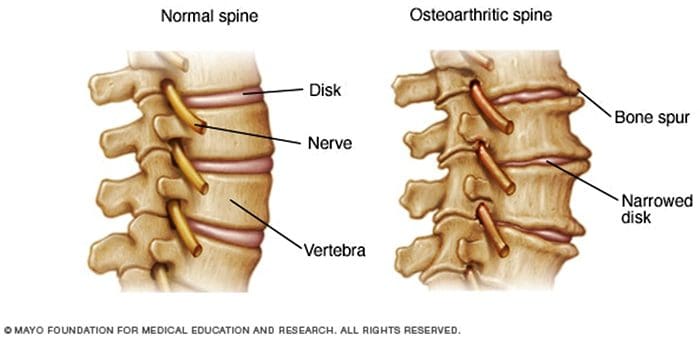
Hay más de 100 diferentes formas de artritis con osteoartritis (OA) siendo la más común. OA es una enfermedad articular progresivamente degenerativa que causa dolor crónico y pérdida de función. Comúnmente, OA es la incapacidad de la articulación para reparar el daño de manera efectiva en respuesta a fuerzas excesivas que se le colocan. Los factores biológicos y psicosociales que comprenden el dolor crónico de OA no se conocen bien, aunque las investigaciones en curso continúan desentrañando la naturaleza compleja de los síntomas de la enfermedad [2]. Las terapias actuales, como los antiinflamatorios no esteroideos (AINE), proporcionan cierto alivio sintomático, reducen el dolor durante períodos cortos de tiempo, pero no alivian el dolor a lo largo de la vida del paciente. Además, las dosis altas de AINE no se pueden tomar repetidamente durante muchos años, ya que esto puede provocar toxicidad renal y hemorragia gastrointestinal.
Tradicionalmente, la investigación de la artritis se ha centrado en gran medida en el cartílago articular como objetivo principal para el desarrollo terapéutico de nuevos fármacos para la OA para la modificación de la enfermedad. Este enfoque "condrocéntrico" ha arrojado nueva luz sobre los intrincados factores bioquímicos y biomecánicos que influyen en el comportamiento de los condrocitos en las articulaciones enfermas. Sin embargo, como el cartílago articular es aneural y avascular, es poco probable que este tejido sea la fuente del dolor de la OA. Este hecho, junto con los hallazgos de que no existe una correlación entre el daño del cartílago articular y el dolor en pacientes con OA [3,4], o en modelos preclínicos de OA [5••, ha provocado un cambio de enfoque desarrollar fármacos para el control eficaz del dolor. Este artículo revisará los últimos hallazgos en la investigación del dolor articular y destacará algunos de los objetivos emergentes que pueden ser el futuro del manejo del dolor de la artritis (resumidos en la Fig. 1)
Citocinas
Las acciones de varias citocinas en estudios de neurofisiología conjunta han aparecido bastante prominentemente recientemente. La interleucina-6 (IL-6), por ejemplo, es una citoquina que típicamente se une al receptor de IL-6 unido a la membrana (IL-6R). IL-6 también puede señalizar al unirse con un IL-6R soluble (sIL-6R) para producir un complejo IL-6 / sIL-6R. Este complejo IL-6 / sIL-6R se une posteriormente a una subunidad transmembrana de glucoproteína 130 (gp130) permitiendo de este modo que IL-6 señalice en células que no expresan constitutivamente IL-6R [25,26] unido a la membrana. Se sabe que IL-6 y sIL-6R son actores clave en la inflamación sistémica y la artritis, ya que se ha encontrado una regulación positiva de ambos en el suero y el líquido sinovial de pacientes con AR. [27-29]. Recientemente, Vázquez et al. observaron que la administración conjunta de IL-6/sIL-6R en las rodillas de ratas provocaba dolor provocado por la inflamación, como lo revela un aumento en la respuesta de las neuronas del asta dorsal de la médula espinal a la estimulación mecánica de la rodilla y otras partes. de la pata trasera [30]. También se observó hiperexcitabilidad de las neuronas espinales cuando se aplicó localmente IL-6/sIL-6R en la médula espinal. La aplicación espinal de gp130 soluble (que "limpiaría" los complejos IL-6/sIL-6R reduciendo así la señalización trans) inhibió la sensibilización central inducida por IL-6/sIL-6R. Sin embargo, la aplicación aguda de gp130 soluble sola no redujo las respuestas neuronales a la inflamación articular ya establecida.
Los canales de potencial de receptor transitorio (TRP) son un grupo de canales de cationes no selectivos que actúan como integradores de diversos procesos fisiológicos y fisiopatológicos. Además de la termosensación, chemosensación y mecanosensación, los canales de TRP están implicados en la modulación del dolor y la inflamación. Se ha demostrado que los canales iónicos TRP vanilloid-1 (TRPV1) contribuyen al dolor inflamatorio articular, ya que la hiperalgesia térmica no fue evocable en ratones TRPV1-/-monoartríticos [31]. De manera similar, los canales iónicos TRP ankyrin-1 (TRPA1) están involucrados en la mecanohipersensibilidad artrítica como bloqueo del receptor con antagonistas selectivos atenuando el dolor mecánico en el modelo adyuvante completo de inflamación de Freund [32,33]. Otras pruebas de que TRPV1 puede estar involucrado en la neurotransmisión del dolor por OA provienen de estudios en los que la expresión de TRPV1 neuronal está elevada en el modelo de OA con monoyodoacetato de sodio [34]. Además, la administración sistémica del antagonista de TRPV1 A-889425 redujo la actividad evocada y espontánea del rango dinámico espinal amplio y las neuronas específicas de la nocicepción en el modelo de monoyodoacetato [35]. Estos datos sugieren que los endovaniloides podrían estar involucrados en los procesos de sensibilización central asociados con el dolor de la OA.
Actualmente se sabe que hay al menos cuatro polimorfismos en el gen que codifica TRPV1, que puede conducir a una alteración en la estructura del canal iónico y la función alterada. Un polimorfismo particular (rs8065080) altera la sensibilidad de TRPV1 a la capsaicina y los individuos que tienen este polimorfismo son menos sensibles a la hiperalgesia térmica [36]. En base a esta anomalía genética, un estudio reciente examinó si los pacientes con OA con el polimorfismo rs8065080 experimentaron una percepción del dolor alterada. El equipo de investigación encontró que los pacientes con OA de rodilla asintomática tenían más probabilidades de portar el gen rs8065080 que los pacientes con articulaciones dolorosas [37]. Esta observación indica que los pacientes con OA con canales TRPV1 de funcionamiento normal tienen un mayor riesgo de dolor en las articulaciones y reafirma la posible participación de TRPV1 en la percepción del dolor OA.
Conclusión
Si bien el obstáculo para tratar el dolor de la artritis sigue siendo eficaz, se están dando grandes pasos en nuestra comprensión de los procesos neurofisiológicos responsables de la generación de dolor en las articulaciones. Se están descubriendo continuamente nuevos objetivos, mientras que los mecanismos detrás de las vías conocidas se están definiendo y refinando aún más. Dirigirse a un receptor específico o canal de iones es poco probable que sea la solución para normalizar el dolor articular, sino que se indica un enfoque de polifarmacia en el que se usan varios mediadores en combinación durante fases específicas de la enfermedad. Desentrañar el circuito funcional en cada nivel de la vía del dolor también mejorará nuestro conocimiento sobre cómo se genera el dolor articular. Por ejemplo, la identificación de los mediadores periféricos del dolor en las articulaciones nos permitirá controlar la nocicepción dentro de la articulación en sí misma y probablemente evitemos los efectos secundarios centrales de los pharamcotherapeutics administrados sistémicamente.
DOLOR FACETÓGENO
 SÍNDROME DE FACETA Y DOLOR FACETOGÉNICO
SÍNDROME DE FACETA Y DOLOR FACETOGÉNICO
- Síndrome de faceta es un trastorno articular relacionado con las articulaciones facetarias lumbares y sus inervaciones, y produce dolor facetogénico tanto local como radiante.
- La rotación excesiva, la extensión o la flexión de la columna vertebral (uso excesivo repetido) pueden provocar cambios degenerativos en el cartílago de la articulación y pueden implicar cambios degenerativos en otras estructuras, incluido el disco intervertebral.
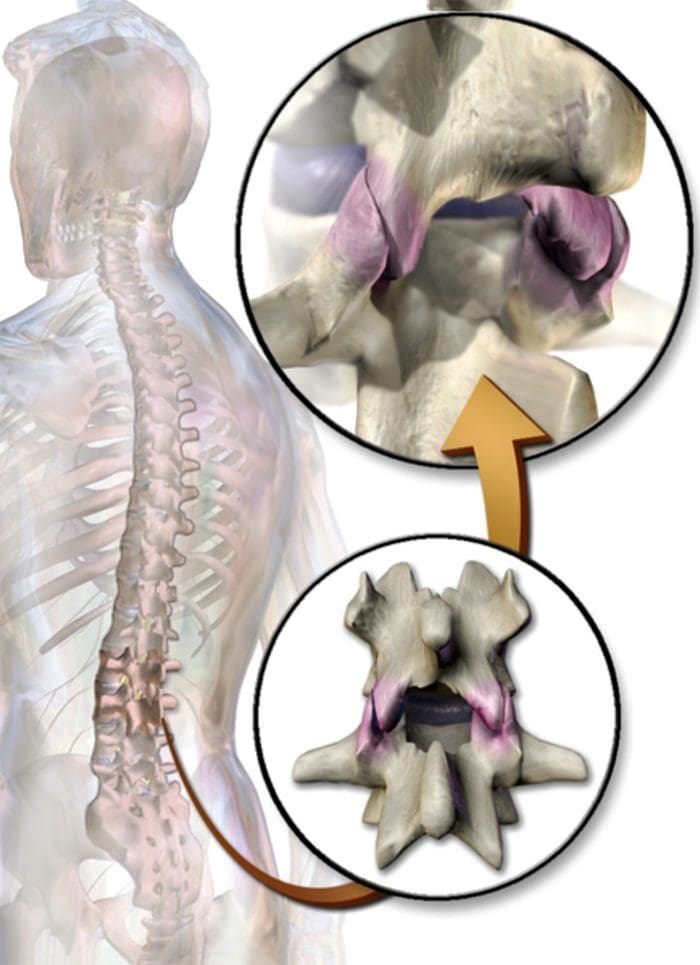
SÍNDROME DE FACETA CERVICAL Y DOLOR FACETOGÉNICO
- Dolor axial en el cuello (rara vez irradia más allá de los hombros), más común unilateralmente
- Dolor con y / o limitación de extensión y rotación
- Ternura a la palpación
- Irradiando el dolor facetogénico localmente o en los hombros o la parte superior de la espalda, y rara vez se irradia en la parte delantera o hacia abajo del brazo o en los dedos como lo haría un disco herniado.
 SÍNDROME DE FACETA LUMBAR Y DOLOR FACETOGÉNICO
SÍNDROME DE FACETA LUMBAR Y DOLOR FACETOGÉNICO
- Dolor o sensibilidad en la parte baja de la espalda.
- Ternura / rigidez local junto a la columna en la parte inferior de la espalda.
- Dolor, rigidez o dificultad con ciertos movimientos (como pararse derecho o levantarse de una silla.
- Dolor al hiperextension
- El dolor referido de las articulaciones facetarias lumbares superiores puede extenderse hacia el flanco, la cadera y el muslo lateral superior
- El dolor referido de las articulaciones facetarias lumbares inferiores puede penetrar profundamente en el muslo, lateralmente y / o posteriormente
- Las articulaciones facetarias L4-L5 y L5-S1 pueden referir dolor que se extiende hacia la pierna lateral distal y, en raras ocasiones, hacia el pie
 EVIDENCIA BASADA EN MEDICINA
EVIDENCIA BASADA EN MEDICINA
Medicina del dolor intervencionista basada en la evidencia de acuerdo con los diagnósticos clínicos
12. Dolor originado en las articulaciones facetarias lumbares
Resumen
Aunque durante mucho tiempo se cuestionó la existencia de un “síndrome facetario”, ahora se acepta generalmente como una entidad clínica. Según los criterios diagnósticos, las articulaciones cigapofisarias representan entre el 5% y el 15% de los casos de lumbalgia axial crónica. Más comúnmente, el dolor facetogénico es el resultado del estrés repetitivo y / o del trauma acumulado de bajo nivel, lo que produce inflamación y estiramiento de la cápsula articular. La queja más frecuente es el dolor lumbar axial con dolor referido percibido en el flanco, la cadera y el muslo. Ningún hallazgo del examen físico es patognomónico para el diagnóstico. El indicador más fuerte del dolor facetogénico lumbar es la reducción del dolor después de los bloqueos anestésicos de las ramas mediales (ramas mediales) de las ramas dorsales que inervan las articulaciones facetarias. Dado que pueden producirse resultados falsos positivos y, posiblemente, falsos negativos, los resultados deben interpretarse con cuidado. En pacientes con dolor en la articulación cigapofisaria confirmado por inyección, las intervenciones de procedimiento pueden realizarse en el contexto de un régimen de tratamiento multidisciplinario y multimodal que incluye farmacoterapia, fisioterapia y ejercicio regular y, si está indicado, psicoterapia. Actualmente, el “estándar de oro” para tratar el dolor facetogénico es el tratamiento con radiofrecuencia (1 B+). La evidencia que respalda los corticosteroides intraarticulares es limitada; por lo tanto, esto debe reservarse para aquellas personas que no responden al tratamiento de radiofrecuencia (2 B1).
El dolor facetogénico que emana de las articulaciones facetarias lumbares es una causa común de dolor lumbar en la población adulta. Golthwaite fue el primero en describir el síndrome en 1911, y generalmente se atribuye a Ghormley la acuñación del término "síndrome facetario" en 1933. El dolor facetogénico se define como el dolor que surge de cualquier estructura que sea parte de las articulaciones facetarias, incluidas las articulaciones fibrosas. cápsula, membrana sinovial, cartílago hialino y hueso.3-5
Más comúnmente, es el resultado de estrés repetitivo y / o trauma acumulado de bajo nivel. Esto conduce a la inflamación, que puede causar que la articulación facetaria se llene de líquido y se hinche, lo que a su vez provoca el estiramiento de la cápsula articular y la consecuente generación de dolor.27 Los cambios inflamatorios alrededor de la articulación facetaria también pueden irritar el nervio espinal a través del estrechamiento del foraminal, lo que produce ciática. Además, Igarashi y cols. 28 descubrieron que las citocinas inflamatorias liberadas a través de la cápsula ventral de la articulación en pacientes con degeneración de la articulación cigogafísica pueden ser parcialmente responsables de los síntomas neuropáticos en individuos con estenosis espinal. Los factores predisponentes para el dolor articular zigagofisial incluyen espondilolistesis / lisis, enfermedad degenerativa del disco y edad avanzada.5
PRUEBAS ADICIONALES IC
La tasa de prevalencia de cambios patológicos en las articulaciones facetarias en el examen radiológico depende de la edad media de los sujetos, la técnica radiológica utilizada y la definición de "anormalidad". Las articulaciones facetarias degenerativas se pueden visualizar mejor a través de un examen de tomografía computarizada (TC).49
DOLOR NEUROPÁTICO

- Dolor iniciado o causado por una lesión o disfunción primaria en el sistema nervioso somatosensorial.
- El dolor neuropático suele ser crónico, difícil de tratar y, a menudo, resistente al tratamiento analgésico estándar.
Resumen
El dolor neuropático es causado por una lesión o enfermedad del sistema somatosensorial, incluidas las fibras periféricas (fibras Aβ, Aδ y C) y las neuronas centrales, y afecta al 7-10% de la población general. Se han descrito múltiples causas de dolor neuropático y es probable que su incidencia aumente debido al envejecimiento de la población mundial, la mayor incidencia de diabetes mellitus y la mejora de la supervivencia del cáncer después de la quimioterapia. De hecho, los desequilibrios entre la señalización somatosensorial excitadora e inhibitoria, las alteraciones en los canales iónicos y la variabilidad en la forma en que se modulan los mensajes de dolor en el sistema nervioso central se han implicado en el dolor neuropático. La carga del dolor neuropático crónico parece estar relacionada con la complejidad de los síntomas neuropáticos, los malos resultados y las difíciles decisiones de tratamiento. Es importante destacar que la calidad de vida se ve afectada en pacientes con dolor neuropático debido al aumento de las prescripciones de medicamentos y las visitas a los proveedores de atención médica, así como a la morbilidad del dolor en sí y la enfermedad desencadenante. A pesar de los desafíos, el progreso en la comprensión de la fisiopatología del dolor neuropático está impulsando el desarrollo de nuevos procedimientos de diagnóstico e intervenciones personalizadas, que enfatizan la necesidad de un enfoque multidisciplinario para el manejo del dolor neuropático.
PATOGENIA DEL DOLOR NEUROPÁTICO
-
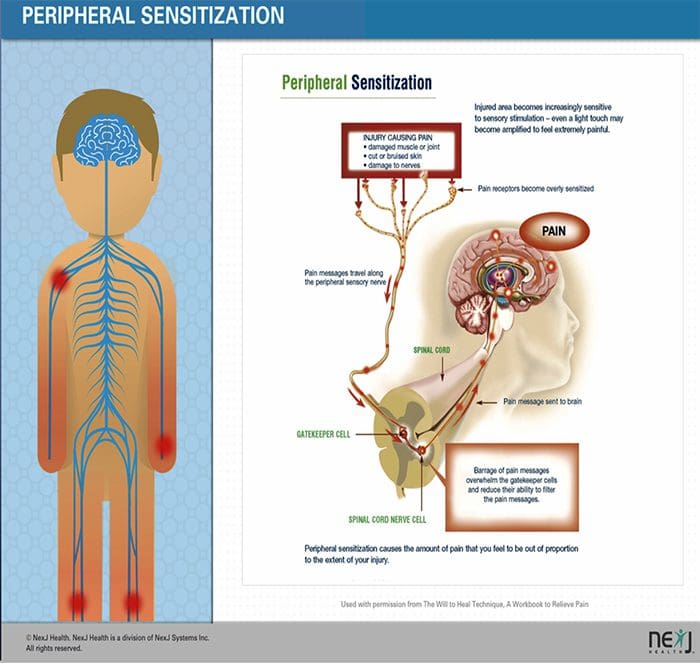
MECANISMOS PERIFÉRICOS
- Después de una lesión del nervio periférico, las neuronas se vuelven más sensibles y desarrollan una excitabilidad anormal y una sensibilidad elevada a la estimulación.
- Esto se conoce como ... ¡Sensibilización periférica!
-
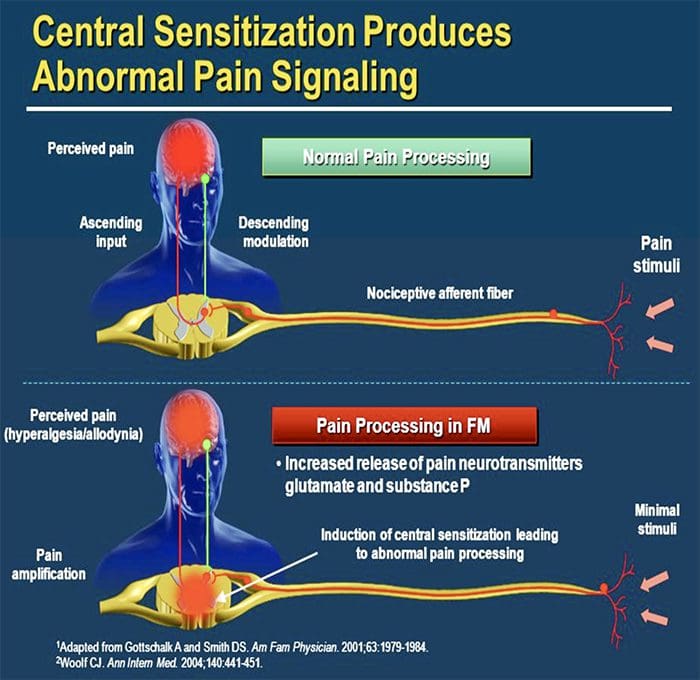
MECANISMOS CENTRALES
- Como consecuencia de la actividad espontánea en curso que surge en la periferia, las neuronas desarrollan una mayor actividad de fondo, campos receptivos ampliados y respuestas aumentadas a los impulsos aferentes, incluidos los estímulos táctiles normales.
Esto se conoce como ... ¡Sensibilización central!
 El dolor neuropático crónico es más frecuente en mujeres (8% frente a 5.7% en hombres) y en pacientes> 50 años (8.9% frente a 5.6% en los menores de 49 años), y afecta con mayor frecuencia a la zona lumbar y las extremidades inferiores. , cuello y miembros superiores 24. Las radiculopatías dolorosas lumbares y cervicales son probablemente la causa más frecuente de dolor neuropático crónico. De acuerdo con estos datos, una encuesta de> 12,000 pacientes con dolor crónico con tipos de dolor tanto nociceptivo como neuropático, remitidos a especialistas en dolor en Alemania, reveló que el 40% de todos los pacientes experimentan al menos algunas características del dolor neuropático (como sensación de ardor, entumecimiento y hormigueo); Los pacientes con lumbalgia crónica y radiculopatía se vieron especialmente afectados25.
El dolor neuropático crónico es más frecuente en mujeres (8% frente a 5.7% en hombres) y en pacientes> 50 años (8.9% frente a 5.6% en los menores de 49 años), y afecta con mayor frecuencia a la zona lumbar y las extremidades inferiores. , cuello y miembros superiores 24. Las radiculopatías dolorosas lumbares y cervicales son probablemente la causa más frecuente de dolor neuropático crónico. De acuerdo con estos datos, una encuesta de> 12,000 pacientes con dolor crónico con tipos de dolor tanto nociceptivo como neuropático, remitidos a especialistas en dolor en Alemania, reveló que el 40% de todos los pacientes experimentan al menos algunas características del dolor neuropático (como sensación de ardor, entumecimiento y hormigueo); Los pacientes con lumbalgia crónica y radiculopatía se vieron especialmente afectados25.
La contribución de la neurofisiología clínica a la comprensión de los mecanismos de cefalea tensional.
Resumen
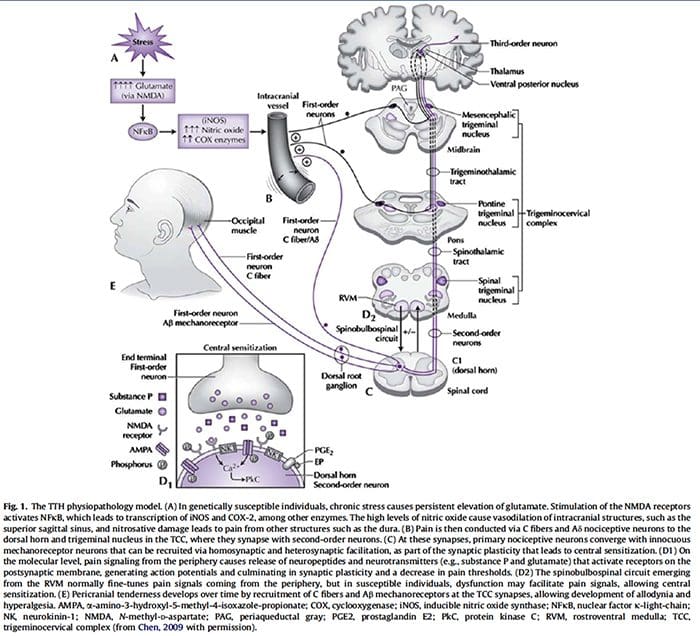
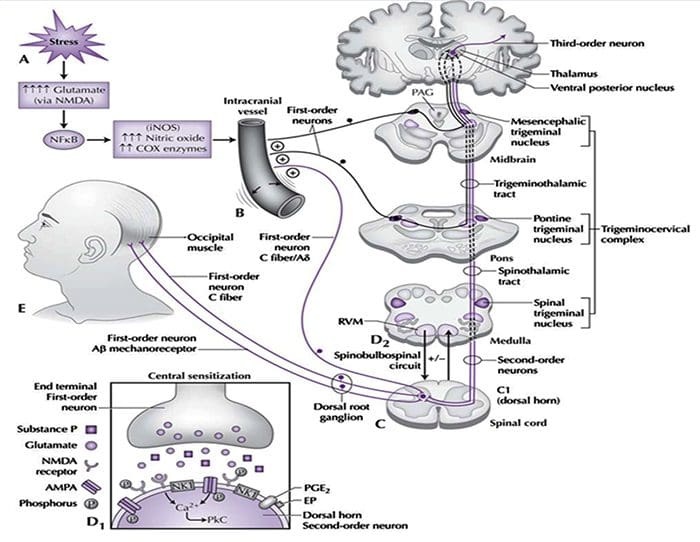
Hasta ahora, los estudios clínicos neurofisiológicos sobre la cefalea tensional (TTH) se han realizado con dos propósitos principales: (1) para establecer si algunos parámetros neurofisiológicos pueden actuar como marcadores de TTH y (2) para investigar la fisiopatología de la TTH. Con respecto al primer punto, los resultados actuales son decepcionantes, ya que algunas anormalidades encontradas en pacientes con TTH se pueden observar con frecuencia también en migrañosos. Por otro lado, la neurofisiología clínica ha jugado un papel importante en el debate sobre la patogénesis de TTH. Los estudios sobre la supresión exteroceptiva de la contracción muscular temporal han detectado una disfunción de la excitabilidad del tronco encefálico y de su control suprasegmental. Se llegó a una conclusión similar al utilizar los reflejos trigeminocervicales, cuyas anormalidades en TTH han sugerido una actividad inhibidora reducida de las interneuronas del tallo cerebral, que reflejan mecanismos anormales de control del dolor endógeno. Es interesante que la anormalidad de excitabilidad neural en TTH parece ser un fenómeno generalizado, no limitado a los distritos craneales. De hecho, los mecanismos similares a DNIC se han evidenciado también en los distritos somáticos mediante estudios de reflejo de flexión nociceptivo. Desafortunadamente, la mayoría de los estudios neurofisiológicos sobre TTH están marcados por serias fallas metodológicas, que deberían evitarse en futuras investigaciones, a fin de aclarar mejor los mecanismos de TTH.
 Referencias:
Referencias:
Neurofisiología del dolor de artritis. McDougall JJ1, Linton P.
www.researchgate.net/publication/232231610_Neurophysiology_of_Arthritis_Pain
Dolor que se origina en las articulaciones facetarias lumbares. van Kleef M1, Vanelderen P, Cohen SP, Lataster A, Van Zundert J, Mekhail N.
Dolor neuropático Luana Colloca,1 Taylor Ludman,1 Didier Bouhassira,2 Ralf Baron,3 Anthony H. Dickenson,4 David Yarnitsky,5Roy Freeman,6 Andrea Truini,7 Nadine Attal,8 Nanna B. Finnerup,9 Christopher Eccleston,10,11 Eija Kalso,12David L. Bennett,13 Robert H. Dworkin,14 y Srinivasa N. Raja15
La contribución de la neurofisiología clínica a la comprensión de los mecanismos de cefalea tensional. Rossi P1, Vollono C, Valeriani M, Sandrini G.
Publicar descargos de responsabilidad
Alcance de la práctica profesional *
La información aquí contenida en "Dolor Facetogénico, Cefaleas, Dolor Neuropático Y Artrosis" no pretende reemplazar una relación personal con un profesional de la salud calificado o un médico con licencia y no es un consejo médico. Lo alentamos a que tome decisiones de atención médica basadas en su investigación y asociación con un profesional de la salud calificado.
Información del blog y debates sobre el alcance
Nuestro alcance informativo se limita a la quiropráctica, musculoesquelética, medicina física, bienestar, contribuyendo etiológico alteraciones viscerosomáticas dentro de las presentaciones clínicas, la dinámica clínica del reflejo somatovisceral asociado, los complejos de subluxación, los problemas de salud delicados y/o los artículos, temas y debates de medicina funcional.
Brindamos y presentamos colaboración clínica con especialistas de diversas disciplinas. Cada especialista se rige por su ámbito de práctica profesional y su jurisdicción de licencia. Utilizamos protocolos funcionales de salud y bienestar para tratar y apoyar la atención de lesiones o trastornos del sistema musculoesquelético.
Nuestros videos, publicaciones, temas, asuntos e ideas cubren cuestiones clínicas, problemas y temas que se relacionan y respaldan directa o indirectamente nuestro ámbito de práctica clínica.*
Nuestra oficina ha intentado razonablemente proporcionar citas de apoyo y ha identificado el estudio o los estudios de investigación relevantes que respaldan nuestras publicaciones. Proporcionamos copias de los estudios de investigación de respaldo disponibles para las juntas reguladoras y el público a pedido.
Entendemos que cubrimos asuntos que requieren una explicación adicional de cómo puede ayudar en un plan de atención o protocolo de tratamiento en particular; por lo tanto, para discutir más a fondo el tema anterior, no dude en preguntar Dr. Alex Jiménez, DC, o póngase en contacto con nosotros en 915-850-0900.
Estamos aquí para ayudarlo a usted y a su familia.
Bendiciones
El Dr. Alex Jimenez corriente continua MSACP, enfermero*, CCCT, IFMCP*, CIFM*, ATN*
email: coach@elpasomedicinafuncional.com
Licenciado como Doctor en Quiropráctica (DC) en Texas & New Mexico*
Número de licencia de Texas DC TX5807, Nuevo México DC Número de licencia NM-DC2182
Licenciada como Enfermera Registrada (RN*) en Florida
Licencia de Florida N.° de licencia de RN RN9617241 (Control No. 3558029)
Estado compacto: Licencia multiestatal: Autorizado para ejercer en 40 Estados*
Matriculado actualmente: ICHS: MSN* FNP (Programa de enfermera practicante familiar)
Dr. Alex Jiménez DC, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Mi tarjeta de presentación digital



 Resumen
Resumen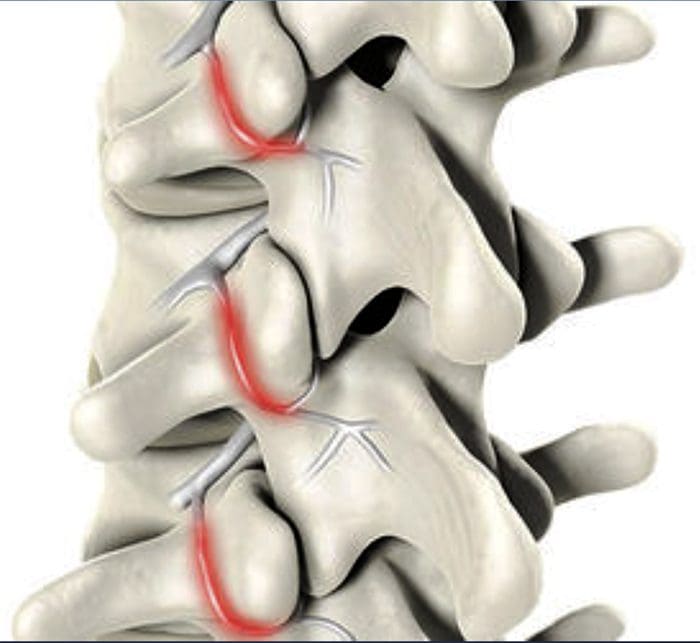 SÍNDROME DE FACETA Y DOLOR FACETOGÉNICO
SÍNDROME DE FACETA Y DOLOR FACETOGÉNICO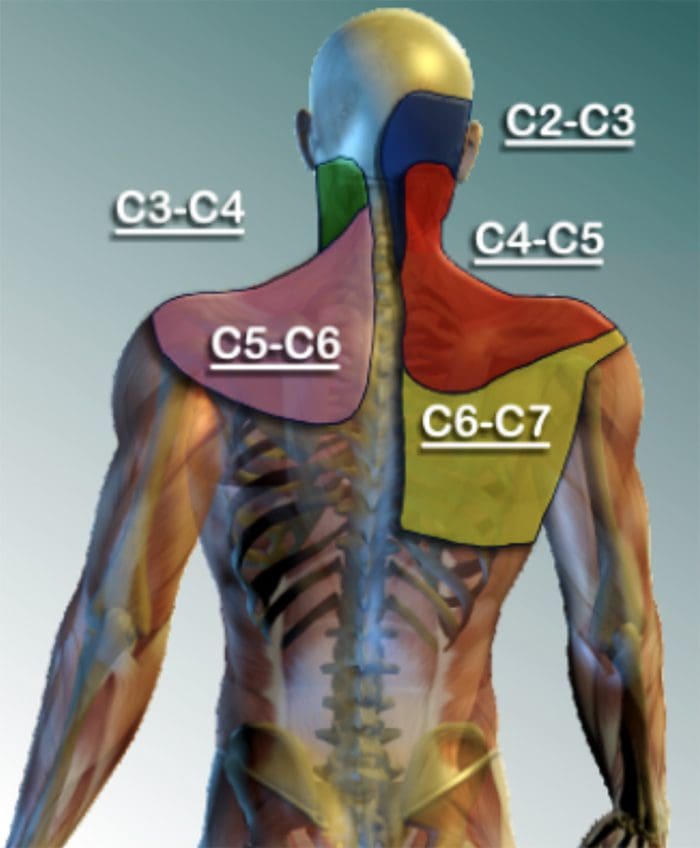 SÍNDROME DE FACETA LUMBAR Y DOLOR FACETOGÉNICO
SÍNDROME DE FACETA LUMBAR Y DOLOR FACETOGÉNICO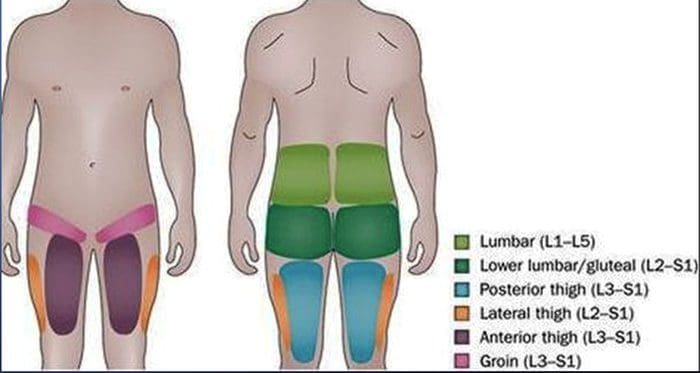 EVIDENCIA BASADA EN MEDICINA
EVIDENCIA BASADA EN MEDICINA


 Referencias:
Referencias:


 De nuevo te doy la bienvenida.
De nuevo te doy la bienvenida.
Los comentarios están cerrados.